Biologische Uhren
Aufgrund der herausragenden elektrochemischen Eigenschaften und hervorragender chemischer Reaktionsträgheit und Biokompatibilität usw., gilt Diamant in Form von dünnen Schichten als ein attraktives Material für (bio-) chemische Sensorik und als Grenzschicht zu biologischen Systemen. Die ultrananokristallinen Diamantfilme werden in unserer Gruppe durch Mikrowellen-assistierter chemischer Gasphasenabscheidung hergestellt, bei der eine Mischung von Methan, als Kohlenstoffquelle, und Stickstoff, als Trägergas, zum Einsatz kommt. Der Film besteht dabei aus Diamantkristalliten, mit Durchmessern unterhalb von 10 nm, die in einer Matrix aus amorphem Kohlenstoff eingebettet sind. Die Oberfläche der Filme ist sehr glatt, mit einer RMS-Rauigkeit von 10 – 14 nm, und mit Wasserstoff terminiert. Die Topografie wird durch rundliche Nanostrukturen mit Durchmessern von etwa 100 nm dominiert. Durch Oberflächenbehandlung mit verschiedenen Plasmen oder photochemischer Prozesse kann die Oberflächen sehr hydrophile (durch O-Terminierung) oder hydrophobe (durch F-Terminierung) Eigenschaften erhalten. Zudem können diese Oberflächenmodifikationen selbst strukturiert werden.
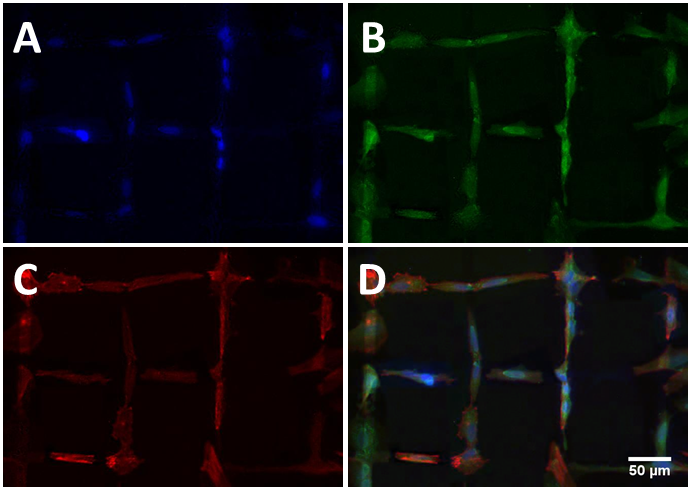
Die Biokompatibilität von UNCD-Filmen wurden durch Kontakttests mit verschiedenen Zelltypen untersucht. Alle Zellen zeigten eine gute Adhäsion und Verbreitung auf den UNCD-Oberflächen nach der Inkubation. Vergleiche mit Zellen von Kontrollproben, nach mehreren Tagen der Kultivierung, zeigten dass die Oberflächen nicht zytotoxisch sind und auch die Vermehrung nicht negativ beeinflusst wird. Weiterhin wurden die Auswirkungen der verschiedenen Oberflächenterminierungen auf die Zellen untersucht. Auf diesen Oberflächen zeigte sich eine verbesserte Bindung der Zellen durch O- oder NH2-Terminierung, was auf die vergrößerte Kontaktfläche der Zellen durch die hydrophilen Eigenschaften dieser Oberflächen zurückzuführen ist [1]. Die Oberflächenrauigkeit ist niedrig genug und in den Dimensionen der Zellen, so dass Sie die Verbreitung der Zellen einengen können, andererseits verbessern Sie die Bindung der Zellen. Die Oberflächenmodifikation beeinflusst die Nanostrukturen nicht [2]. Die Strukturierung der Oberflächenterminierung kann dazu genutzt werden die Bindung und das Wachstum der Zellen zu kontrollieren (siehe Abbildung) [3].
Die UNCD-Oberfläche kann zudem mit Proteinen oder Nukleinsäuren durch verschiedenste chemische Kopplungsrouten funktionalisiert werden, je nach Oberflächenterminierung. Zum Beispiel konnten wir zum einen die Bindung von dsRNA auf UNCD-Oberflächen zeigen, welche durch Thiolgruppen terminierte DNA funktionalisiert wurden, zum anderen die kovalente Bindung von Esterase und die nicht-kovalente Bindung von Lipase auf UNCD [4].
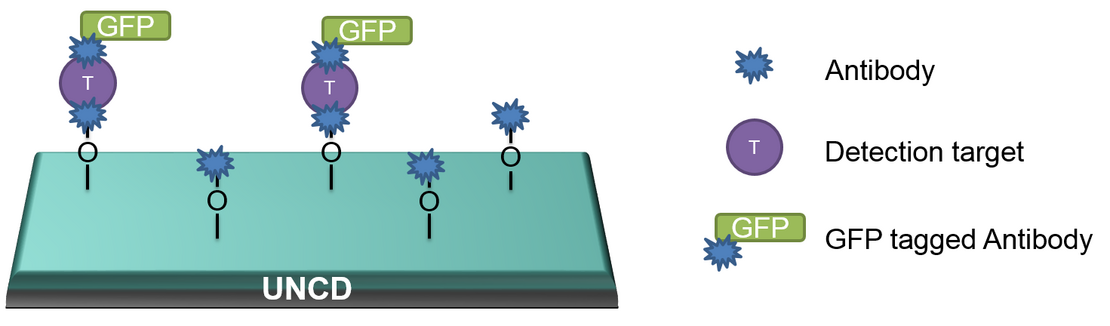
Das Ziel unseres Projekts ist die Herstellung von UNCD basierten Plattformen, für zeitaufgelöste Fluoreszenzstudien von neuronalen Signalen. Die UNCD-Oberfläche wird dazu modifiziert und strukturiert, um bestimmte Bereiche zu definieren mit verbesserter Zelladhäsion. Die Oberfläche um eben diese Bereiche soll mit den entsprechenden Antikörpern funktionalisiert werden, um die von den Neuronen freigesetzten Ziele, Neurotransmitter (Acetylcholin, Serotonin) und Neuropeptide (Pigment Dispersing Factor, PDF), zu binden. Diese Ziele werden mit einem GFP (Grün fluoreszierenden Protein) getaggten Antikörper markiert und detektiert mit einem Konfokalmikroskop, innerhalb eines bestimmten Zeitrahmens (siehe Abbildung). Als Alternative zu diesem sogenannten Sandwich-Konstrukt (Ziel muss von zwei Antikörpern gebunden werden), können kompetitive Assays dienen (bspw. für Serotonin). Das Projekt wird in Kooperation mit der Abteilung für Tierphysiologie und der Abteilung für Biochemie realisiert.
Projekt Partner
- Prof. Dr. Monika Stengl, Dept. of Tierphysiologie
- Prof. Dr. Arno Müller, Dept. of Entwicklungsgenetik
- Prof. Dr. Olaf Stursberg, Dept. of Regelungs- und Systemtheorie
- Prof. Dr. Raffael Schaffrath, Dept. of Mikrobiologie
- Prof. Dr. Georg Mayer, Dept. of Zoologie
- Prof. Dr. Jörg Kleinschmidt, Dept. of Biophysik
- Prof. Dr. Markus Maniak, Dept. of Zellbiologie
- Prof. Dr. Friedrich Herberg, Dept. of Biochemie
- Prof. Dr. Martin Garcia, Dept. of Theoretische Physik
- Prof. Dr. Thomas Fuhrmann-Lieker, Dept. of Physikalische Chemie
Bildergalerie